Всё о HER2-позитивном раке молочной железы.
HER2-позитивный статус при раке молочной железы указывает на то, что раковые клетки содержат повышенное количество рецепторов эпидермального фактора роста 2-го типа (HER2) на своей поверхности.
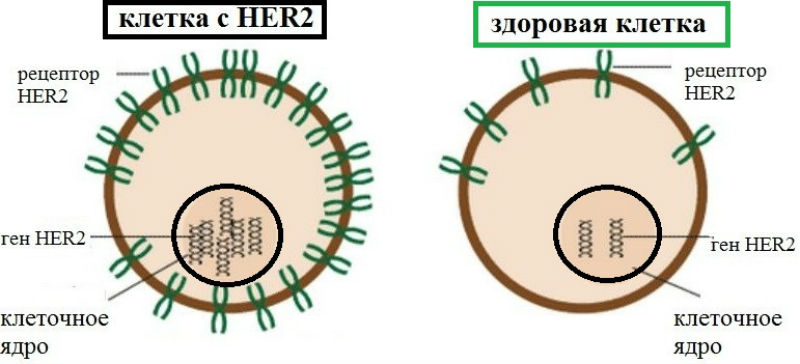
Это состояние, известное как "положительный HER2-статус", встречается примерно у 15-20% пациенток с раком молочной железы.
Рецептор HER2 обычно присутствует в здоровых тканях и играет ключевую роль в регулировании процессов деления и дифференциации клеток. Однако его избыточное количество может способствовать более агрессивному росту и распространению раковых клеток.
Для диагностики статуса HER2 используют трепанбиопсию опухоли молочной железы с иммуногистохимическим исследованием (ИГХ)
Результат , которого показывает:
Гормональные рецепторы: Рецепторы к эстрогенам (ER) и прогестерону (PR) важны для определения эффективности гормональной терапии у пациентов. Опухоли, положительные на эти гормоны, обычно имеют более благоприятный прогноз, менее склонны к метастазированию и чаще обнаруживают метастазы в костной ткани. При таких формах рака наблюдается более высокий процент пятилетней выживаемости по сравнению с другими подтипами.
HER2: Примерно в 20% случаев рака молочной железы наблюдается увеличенное производство белка HER2, что делает опухоль более агрессивной и склонной к быстрому прогрессированию. Однако такие опухоли чувствительны к специфическим таргетным терапиям.
Ki-67: Уровень белка Ki-67 коррелирует с пролиферативной активностью клеток, то есть с их способностью к делению. Высокий уровень Ki-67 указывает на более активное деление клеток и может служить врачу индикатором агрессивности опухоли. Опухоли с высокой пролиферативной активностью обычно хорошо отвечают на химиотерапию.

Терапевтические подходы к лечению HER2-позитивного рака молочной железы
HER2 представляет собой рецепторный белок, расположенный на поверхности клеток. В нормальных условиях он регулирует рост и развитие клеток. Однако при раке молочной железы может происходить гиперэкспрессия HER2, что приводит к неконтролируемому делению клеток. Определение уровня HER2 критично для выбора стратегии лечения.
Таргетная терапия для HER2-позитивного рака
Таргетная терапия направлена на точечное воздействие на определённые молекулярные цели. В контексте HER2-позитивного рака, анти-HER2 препараты специфически атакуют избыточные рецепторы, присутствующие в опухолевых клетках.
Это снижает токсичность по сравнению с традиционной химиотерапией и является частью интегрированного подхода к лечению, учитывающего стадию заболевания и другие факторы.
Препараты анти-HER2
К анти-HER2 препаратам относятся инъекционные формы (такие как трастузумаб, пертузумаб, трастузумаб эмтанзин, трастузумаб дерукстекан) и оральные медикаменты (например, лапатиниб).
Дополнительные терапевтические меры
При сочетании повышенной экспрессии HER2 с гормонозависимым раком, гормональная терапия может быть включена в лечебный режим.
Лечение на разных стадиях
Если опухоль ограничена молочной железой и близлежащими лимфоузлами и не дала метастазов, цель лечения — полностью избавить организм от опухолевых клеток.
В зависимости от размера опухоли и наличия метастазов в лимфоузлах, могут быть рекомендованы различные подходы:
Для опухолей размером менее 2 см без метастазов в лимфоузлах: хирургическое удаление с последующей адъювантной химио-таргетной терапией;
Если опухоль превышает 2 см или есть метастазы в лимфоузлах: неоадъювантная химио-таргетная терапия перед операцией, за которой следует хирургическое вмешательство и адъювантная таргетная терапия.
Лучевая терапия применяется для предотвращения местного рецидива и зависит от размера первичной опухоли, типа операции и состояния лимфоузлов. При гормонозависимом раке назначается гормональная терапия.
Неоадъювантная терапия предполагает начальное применение медикаментозного лечения для уменьшения опухоли перед рассмотрением возможности хирургического вмешательства.
Существуют два основных подхода к неоадъювантной терапии, выбор между которыми зависит от общего состояния пациента, возраста и сопутствующих заболеваний.
Наиболее эффективным считается протокол лечения, включающий комбинацию двух химиотерапевтических препаратов (доцетаксел и карбоплатин) и двух таргетных анти-HER2 препаратов (трастузумаб и пертузумаб), которые усиливают действие друг друга, повышая шансы на уменьшение размеров опухоли.
Этот курс химио-таргетной терапии проводится каждые три недели на протяжении шести циклов, с контролем эффективности лечения через УЗИ и/или маммографию после каждых трех циклов.
Ограничения на использование этого метода включают пожилой возраст пациента и наличие серьезных сопутствующих заболеваний.
В случае противопоказаний к основной терапевтической схеме, возможен переход на альтернативный курс, включающий два этапа.
На первом этапе применяется комбинация доксорубицина и циклофосфамида (применяемая один раз каждые две или три недели на протяжении четырех циклов), после чего проводится оценка результативности лечения и, при положительной динамике, осуществляется переход к комбинированной химио-таргетной терапии, включающей таксан, трастузумаб и пертузумаб на срок до 12 недель.
По завершении неоадъювантной химиотерапии возникает вопрос о необходимости хирургического вмешательства, объем которого определяется исходными размерами опухоли, степенью поражения лимфатических узлов и общим эффектом предшествующей терапии.
После хирургической операции материал молочной железы направляется на гистологическое и иммуногистохимическое исследование. В зависимости от реакции на неоадъювантную терапию (полный ответ характеризуется отсутствием опухолевых клеток в тканевом образце, в то время как неполный ответ свидетельствует о наличии остаточной опухоли в удаленной ткани молочной железы или лимфатических узлах), принимается решение о дальнейшем адъювантном лечении.

Адъювантная терапия
Такое лечение, проводимое после операции, рекомендуется всем пациентам с HER2-позитивным раком молочной железы.
В случае полного ответа на предшествующую химио-таргетную терапию и операцию, стандартной практикой является назначение трастузумаба (применяемого один раз в три недели на протяжении года).
Продолжительность такой адъювантной таргетной терапии считается оптимальной, так как шестимесячный курс оказался менее эффективным в долгосрочной перспективе, а двадцатичетырехмесячный курс не показал значительного улучшения по сравнению с двенадцатимесячным.
Перед операцией, если была проведена двойная блокада HER2-рецепторов с использованием трастузумаба и пертузумаба, рекомендуется продолжить такую же терапию после хирургического вмешательства на протяжении года.
В случае, когда после терапии не наблюдается полного излечения и остаются участки опухоли, устойчивые к трастузумабу, показано назначение трастузумаб эмтанзина. Препарат применяется каждые три недели на протяжении первого года лечения, всего 14 циклов.
Пациентам, которым не проводилась неоадъювантная терапия из-за ограниченного распространения опухоли и которые подверглись операции, может быть предложена химио-таргетная терапия на основе паклитаксела и трастузумаба после подтверждения диагноза гистологическим исследованием. Для случаев более широкого распространения заболевания, например, при поражении лимфоузлов, возможно добавление пертузумаба.

Лечение метастатического HER2-позитивного рака молочной железы включает анти-HER2 терапию и химиотерапию, которые применяются в различных комбинациях и последовательности.
Оптимальный первичный курс лечения состоит из комбинации таксана (чаще всего доцетаксела), трастузумаба и пертузумаба. Лечение является длительным, и химиотерапевтический компонент (таксан) может быть исключен из схемы через несколько месяцев в зависимости от реакции пациента и для снижения риска токсичности.
Тем не менее, прием анти-HER2 препаратов продолжается до тех пор, пока они оказывают терапевтический эффект, то есть до прогрессирования болезни или появления серьезных побочных эффектов.
При замедленном развитии заболевания и при раке, зависимом от гормонов, врач может предложить терапию без использования химиотерапевтических средств. В таких случаях, наряду с анти-HER2 медикаментами, пациенту назначается гормональное лечение.
Среди ключевых достоинств таргетных лекарств выделяется их способность преодолевать гематоэнцефалический барьер, что позволяет оказывать влияние на метастазы в мозге.
С развитием болезни могут быть задействованы дополнительные препараты, такие как трастузумаб эмтанзин, лапатиниб в сочетании с капецитабином, трастузумаб дерукстекан.
Также возможно повторное использование ранее применяемых анти-HER2 медикаментов, например, трастузумаба, и препаратов, еще не утвержденных в России, доступных в рамках клинических испытаний.
Побочные эффекты анти-HER2 терапии.
Побочные эффекты от анти-HER2 лекарств, хоть и схожи с теми, что возникают от химиотерапии, проявляются реже и менее интенсивно благодаря целенаправленному воздействию на определенные клетки, в частности, на опухолевые. Основные побочные эффекты включают:
кардиотоксичность — негативное воздействие на сердечную мышцу,
сыпь,
диарея.
Влияние на сердце может быть бессимптомным, с уменьшением функции органа, обнаруживаемым только при эхокардиографии (эхоКГ = УЗИ сердца).
В некоторых случаях пациенты могут испытывать симптомы, свойственные сердечной недостаточности. Повреждение сердца обычно обратимо, но из-за риска кардиотоксичности необходимо проводить эхоКГ каждые три месяца во время анти-HER2 терапии.
Исследование показало, что в определённых случаях таргетная терапия может быть временно остановлена. В такие периоды возможно назначение терапии для лечения сердечной недостаточности.
Продолжение таргетной анти-HER2 терапии рассматривается после улучшения функции левого желудочка, при условии, что преимущества лечения перевешивают потенциальные риски.
Наблюдается, что сыпь чаще возникает при использовании пертузумаба, развиваясь примерно в 24% случаев. Диарея чаще ассоциируется с препаратами лапатиниб (55%) и пертузумаб (28–72%).
Выводы:
Таргетная терапия открывает новые возможности для эффективного лечения рака молочной железы с повышенной экспрессией HER2.
Анти-HER2 таргетная терапия применима на разных этапах развития заболевания.
Возможно сочетание анти-HER2 таргетной терапии с химио- или гормонотерапией.
Анти-HER2 таргетная терапия эффективна против метастазов в мозге.