Гормонозависимый рак молочной жлезы.
Гормонозависимый рак молочной железы.
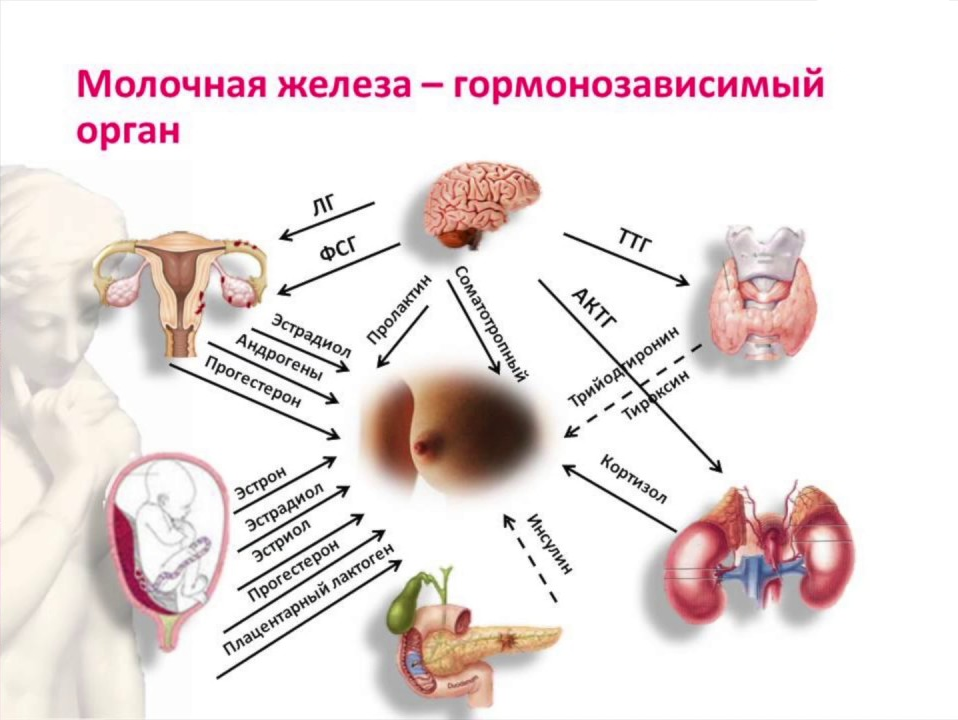
Гормонозависимый рак молочной железы представляет собой не единичное заболевание, а целую категорию опухолевых процессов, объединенных разнообразием клеточных трансформаций и различной чувствительностью к гормональным воздействиям. Общим фактором для этих многочисленных форм рака является их реакция на гормоны.
Статистика:
В 2019 году в России было зарегистрировано 73,366 случаев рака молочной железы среди женщин. Примечательно, что 44% из этих случаев были обнаружены благодаря профилактическим обследованиям, без каких-либо подозрений со стороны пациенток. На данный момент под медицинским наблюдением находятся 446,077 женщин, которые успешно прошли первичное лечение и прожили с диагнозом более пяти лет.
Данные также показывают, что 65% женщин после менопаузы подвержены риску развития гормонозависимой карциномы. Хотя официальная статистика не разделяет случаи рака молочной железы по типам, можно предположить, что из 50,000 женщин старше 50 лет (средний возраст наступления менопаузы), примерно 32,000 столкнутся с гормонозависимым раком молочной железы, что составляет около половины всех диагностированных случаев.
Стоит отметить, что у носителей гена BRCA2 вероятность развития гормонозависимой карциномы выше, особенно если рак молочной железы проявляется в молодом возрасте, в отличие от случаев с мутациями гена BRCA1.
Формы и виды:
Рак молочной железы выделяется в онкологии благодаря широкому спектру терапевтических методов, которые способствуют продлению жизни и улучшению её качества.
Изначально классификация основывалась на наличии гормональных рецепторов в опухолевых клетках, а последующее молекулярное типирование позволило персонализировать лечение, учитывая генетические характеристики опухоли.
Гормональная чувствительность рака молочной железы определяется присутствием рецепторов к эстрогенам (ER). Наличие прогестероновых рецепторов (PR) не является обязательным, но может повысить эффективность терапии и улучшить прогноз.
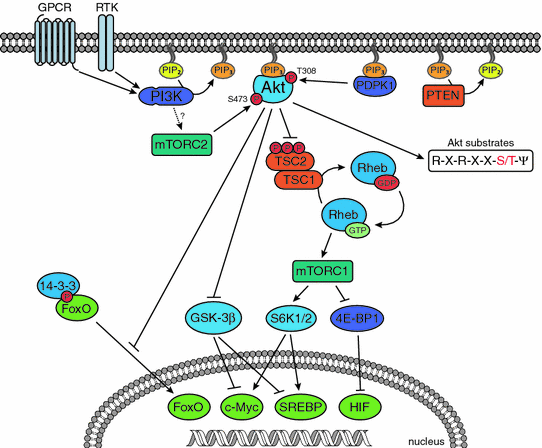
Для классификации опухоли как гормонозависимой достаточно наличия ER или PR хотя бы в 10% клеток.
Оказывается, что в реальных клинических условиях у 45% женщин с положительным статусом эстрогеновых рецепторов (ER) отсутствует реакция на антигормональную терапию.
Высокие уровни ER также не являются абсолютной гарантией эффективности, поскольку у 10% пациенток с высоким содержанием ER терапия не приносит ожидаемых результатов.
Даже при комбинации высоких уровней ER и прогестероновых рецепторов (PR) у каждой пятой женщины отсутствует положительный эффект от лечения.
Это указывает на то, что опухоль может быть независимой от гормонов, несмотря на классификацию как люминальный тип.
В таких случаях может потребоваться протокол лечения, предназначенный для гормон-нечувствительного рака.
Следовательно, рак молочной железы (РМЖ) целесообразнее классифицировать на основе его реальной чувствительности к терапии.
В контексте биологической типизации РМЖ, наличие ER необходимо для определения люминального карциномы, в то время как отсутствие ER характерно для трижды негативного и базального рака молочной железы.
Тем не менее, примерно треть пациенток с раком молочной железы не соответствует ни одной из установленных категорий, что подчеркивает необходимость дополнительных исследований неизвестных типов рака.
Морфологическая классификация рака молочной железы включает множество клеточных вариантов, однако выбор метода лечения всегда зависит от гормональной чувствительности опухоли.
Поэтому разделение опухолей на гормонозависимые и гормон-рецептор-отрицательные типы остается ключевым и практически важным для определения лечебной стратегии.
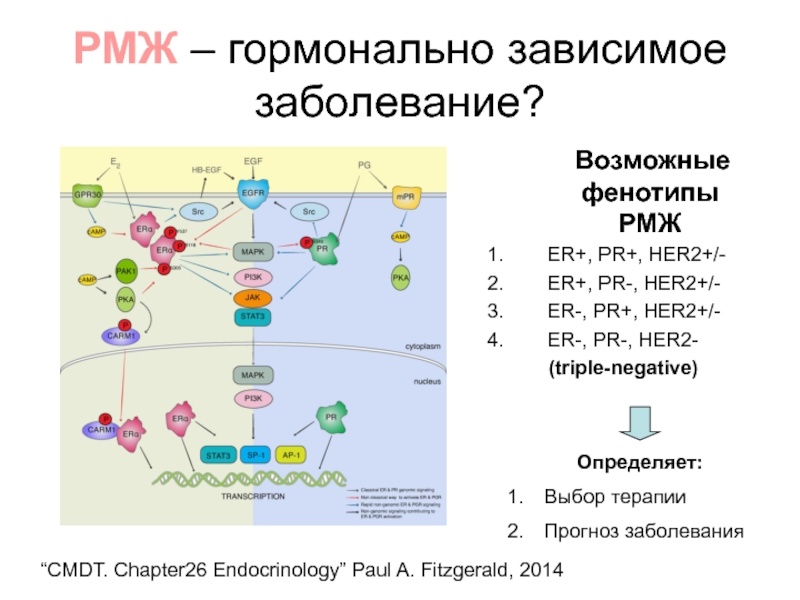
Люминальный тип рака молочной железы классифицируется на две основные категории:
- Люминальный тип А обычно определяется присутствием ER (рецепторов эстрогена) и PR (рецепторов прогестерона), отсутствием HER2 и низким уровнем Ki-67. Этот подтип является наиболее распространенным среди раков молочной железы.
- Люминальный тип В характеризуется наличием рецепторов эстрогена на клеточной поверхности, в то время как рецепторы прогестерона могут быть отсутствующими. Уровень Ki-67 при этом высокий. Этот подтип встречается реже, составляя около 20% случаев.
Для диагностики гормонозависимого рака молочной железы ключевым является проведение трепан-биопсии с последующим гистологическим и иммуногистохимическим анализом, включая тесты на рецепторы эстрогена и прогестерона, HER2 и Ki-67. Это позволяет подтвердить злокачественность новообразования и определить стратегию лечения.
Необходимы также маммография, УЗИ молочных желез и исследование зон регионарного лимфооттока.
Для определения стадии заболевания и выявления метастазов используются различные методы диагностики.
Компьютерная томография (КТ) и рентгенография грудной клетки, а также КТ и ультразвуковое исследование (УЗИ) брюшной полости и органов малого таза позволяют оценить распространенность опухоли.
В случае подозрения на метастазы в костях или головном мозге, могут быть назначены остеосцинтиграфия и магнитно-резонансная томография (МРТ) или КТ головного мозга.
При наличии клинических показаний проводится молекулярно-генетическое тестирование на мутации генов BRCA1/2, которые связаны с наследственным риском развития рака молочной железы.
Терапия люминального типа рака молочной железы включает в себя мультидисциплинарный подход.
Консилиум специалистов, в который входят хирург, онколог-химиотерапевт и радиотерапевт, определяет стратегию лечения. В зависимости от возможности радикального удаления опухоли, лечение может начинаться с хирургического вмешательства, за которым следует адъювантная (профилактическая) лекарственная и лучевая терапия.
Если опухоль первоначально не поддается резекции (удалению), применяется неоадъювантная (предоперационная) терапия для уменьшения её размеров, после чего проводится операция и, при необходимости, назначается дополнительная адъювантная терапия и лучевое лечение.
В случае метастатического поражения внутренних органов и костей скелета осуществляется системная лекарственная терапия и симптоматическое лечение.
В лечении люминального рака молочной железы (РМЖ) применяется гормонотерапия, основанная на наличии рецепторов к эстрогену и прогестерону на клетках опухоли.
Этот метод может использоваться как до, так и после оперативного вмешательства, адаптируясь под индивидуальные характеристики пациента.
В случае, если опухоль перестаёт реагировать на гормонотерапию, врачи могут перейти к химиотерапии.
Выбор конкретных гормональных препаратов зависит от множества параметров, включая гормональный статус женщины.
В период пременопаузы основным источником эстрогенов являются яичники, тогда как в менопаузе эстрогены в основном вырабатываются периферическими тканями, такими как жировая ткань и надпочечники. Это влияет на механизм действия и выбор препаратов для разных групп пациентов.
В гормонотерапии РМЖ используются различные группы препаратов:
Антиэстрогены:
Тамоксифен, торемифен и фулвестрант являются примерами антиэстрогенов, которые блокируют действие эстрогенов на клетки, связываясь с их рецепторами. Эти препараты часто применяются у пациенток в период пременопаузы и обычно не требуют подавления функции яичников.
Прием антиэстрогенных препаратов может сопровождаться различными побочными эффектами.
Женщины могут испытывать симптомы, схожие с менопаузой, включая всплески тепла, головные боли, изменения в менструальном цикле и сухость слизистых оболочек.
Существует также риск тромбоэмболических осложнений, особенно при наличии предрасполагающих факторов.
Влияние на эндометрий может привести к гиперплазии, образованию полипов и, в очень редких случаях, к раку эндометрия.
Другие возможные побочные эффекты включают мышечные и костные боли, общую слабость, ухудшение состояния волос и зрения, в том числе снижение остроты зрения и усугубление катаракты.
Ингибиторы ароматазы, используемые для лечения люминального рака молочной железы, блокируют синтез эстрогенов в периферических тканях, не воздействуя на их производство в яичниках. Эти препараты обычно назначаются женщинам в период менопаузы.
Хирургическое вмешательство, такое как овариэктомия, является необратимым методом лечения.
Для временного подавления функции яичников применяются специфические медикаменты – агонисты гонадотропин-релизинг-гормона, включая гозерелин, бусерелин и лейпрорелин.
Важно учитывать, что действие этих лекарственных средств наступает не мгновенно, и у некоторых молодых женщин может не произойти полное подавление функции яичников.
При использовании агонистов ГрГ возможно развитие симптомов менопаузы.
Ингибиторы CDK 4/6, такие как палбоциклиб, рибоциклиб и абемациклиб, широко применяются в лечении метастатического гормончувствительного рака молочной железы.
Эти препараты блокируют клеточный цикл, ингибируя ферменты циклинзависимые киназы, ответственные за переход клетки из одной фазы цикла в другую.
Прием данных медикаментов может привести к изменениям в клиническом анализе крови, включая лейкопению, нейтропению и тромбоцитопению, а также увеличивает риск сердечно-сосудистых заболеваний и гепатотоксичности, что проявляется повышением уровней трансаминаз, билирубина в крови, а также тошнотой, рвотой и диареей.
Для предотвращения побочных эффектов гормонотерапии, врач должен оценить все связанные риски.
Пациентам необходимо сообщать о всех хронических заболеваниях и принимаемых лекарствах, а также активно лечить любые сопутствующие заболевания.
Для изменения образа жизни рекомендуется прекратить курение и употребление кофеина, минимизировать стресс, а также регулярно заниматься физическими упражнениями. Поддержание здорового веса и сбалансированное питание также играют важную роль.
В случае трудно переносимых симптомов менопаузы, врач может предложить медикаментозное лечение, включая препараты с антиконвульсивным и антидепрессивным действием, а также фитопрепараты с эффектом, схожим с эстрогеном.
Для женщин с повышенным риском остеопороза могут быть рекомендованы остеомодифицирующие препараты, такие как бисфосфонаты (например, золедроновая кислота), деносумаб, витамин D и кальций.
Посещение гинеколога рекомендуется ежегодно, а в случае гинекологических заболеваний — частота и объем обследований определяются лечащим врачом.
Список литературы:
1. "Злокачественные новообразования в России в 2021 году", под редакцией А.Д. Каприна, В.В. Старинского. Москва: МНИОИ им. П.А. Герцена - филиал ФГБУ "НМИЦ радиологии" Минздрава России, 2022.
2. Тюляндин С.А., Жукова Л.Г., Королева И.А. и др. "Практические рекомендации по лекарственному лечению рака молочной железы". Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2021, том 11.
3. Клинические рекомендации Ассоциации онкологов России (АОР), утвержденные Минздравом России в 2022 году "Рак молочной железы".
4. "Breast Cancer, Version 4.2022", NCCN Clinical Practice Guidelines in Oncology, Journal of the National Comprehensive Cancer Network, 2022.
5. ESMO Clinical Practice Guidelines for Early Breast Cancer, ESMO, 2022.
6. Семиглазова Т.Ю., Берлев И.В., Ульрих Е.А. и др. "Протективная и лечебная роль овариальной супрессии при раннем раке молочной железы".